Con la entrada de hoy finalizamos la serie sobre retinopatía diabética. En el primero hablamos de cómo se forman las lesiones, y en el segundo qué consecuencias tienen para la visión. Hablamos de dos lesiones básicas que van a tener malas consecuencias para la función del ojo: el edema macular y la formación de neovasos.
Para ambos problemas, el tratamiento estrella es el láser.

Se llama fotocoagulación porque por medio de la luz («foto-«) que es el láser, coagulamos las proteínas de algunas células en la retina. Coagular no se refiere siempre a que se forme un coágulo en la sangre, sino que ciertas proteínas pierden su conformación espacial y dejan de funcionar. Es una quemadura muy localizada, que producirá diferentes efectos según dónde lo utilicemos. En este artículo antiguo explicamos los diferentes tratamientos láser en el ojo, y también describimos la fotocoagulación en la retina. Además, en este otro artículo sobre el desprendimiento de retina, explicábamos como «sellar» los agujeros retinianos con el láser.
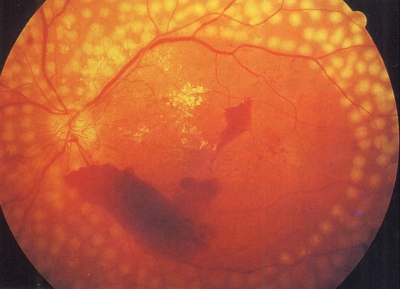
Edema macular
En este caso el tratamiento láser busca un efecto diferente que «quemar la retina» para sujetarla al tejido de atrás. Recordamos que el edema macular supone un acúmulo de líquido (principalmente agua) en la parte central de la retina, que es la que usamos en la visión fina. Este fluido sale de lesiones vasculares en las que se escapa líquido desde el torrente sanguíneo. Primero debemos identificar estos puntos donde se origina el edema, estas zonas de fuga de líquido. Normalmente son microaneurismas, que podemos ver a simple vista en el fondo del ojo. Además, decíamos que los exudados duros son un signo indirecto de edema. De hecho, el propio edema, como engrosamiento de la retina, lo podemos ver también en el fondo de ojo si el oftalmólogo tiene la suficiente experiencia en retina. Por tanto, en algunos casos la «simple» observación de fondo de ojo nos da pistas de qué puntos originan el edema macular. Sin embargo, el estudio del edema macular se hace mejor (y por lo tanto, las posibilidades de éxito del tratamiento suben) si nos ayudamos de pruebas complementarias. Estoy hablando de la tomografía de coherencia óptica (OCT) y de la angiofluoresceingrafía (AFG).
De la OCT estuvimos hablando en el artículo anterior: nos da imágenes de alta resolución de la retina, como si hubiéramos hecho cortes retinianos y los miráramos al microscopio. Es el sistema ideal para encontrar edema macular, cuantificarlo (eso nos servirá para comprobar más tarde el resultado del tratamiento) y localizarlo (podemos hacer un «mapa macular», teniendo información objetiva del espesor de la retina en las diferentes zonas de la mácula).
De la AFG estuvimos hablando en el artículo sobre la coroidopatía serosa central. Explicábamos que es un tipo de angiografía, una forma de estudiar los vasos sanguíneos gracias a que metemos un contraste intravenso que «colorea» las venas y arterias. El colorante está confinado dentro de los vasos sanguíneos siempre que estos sean normales. Cuando hay zonas de «fuga» (posible origen del edema macular), el contraste difunde lentamente fuera del árbol vascular.
Por tanto, la OCT nos muestra dónde están las áreas de edema, y la AFG nos señala concretamente los microaneurismas u otras lesiones que dejan escapar el colorante (y por tanto, agua). Puestos a elegir, lo ideal es complementar la exploración de fondo de ojo con ambas pruebas. Ya que aunque la AFG nos señala todos los puntos de fuga, no todos son responsables del edema macular. Y la OCT nos señala la zona de edema macular, pero no nos señala exactamente la lesión. En ocasiones, el oftalmólogo no tiene tan fácil acceso a alguno de estos métodos, y eso no quiere decir que no pueda tratar el edema macular. Como todo, la práctica clínica se adapta a los recursos disponibles.
Fotocoagulación focal
Vale, de una forma u otra hemos identificado las lesiones a tratar. ¿Cómo lo hacemos?. Se trata de cerrar esa alteración vascular, ese microaneurisma o ese vaso anómalo que deja escapar líquido. Apuntando directamente con el láser y aplicando calor, la lesión se coagula realmente, se cierra. Con esto, si tenemos suerte, el edema mejora. Eso significa que en un tiempo (la revisión se debe demorar, no se puede evaluar en unos días) el grosor retiniano disminuye.
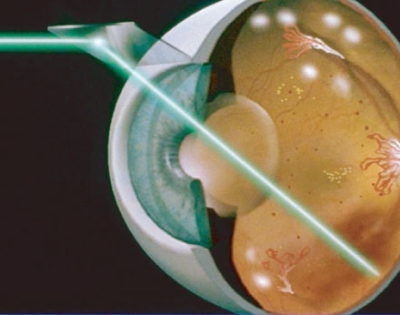
Hay que tener en cuenta que dar láser sobre la mácula requiere precaución. El centro de la mácula (la fóvea) es «intocable», no podemos impactar ahí porque la quemadura puede producir una pérdida visual irreversible. Además, las cicatrices del láser crecen con el tiempo, así que tampoco podemos quedarnos «justo al lado del centro» con el láser, tenemos que dejar un margen de seguridad. Por otra parte, si de por sí la diabetes supone un aporte sanguíneo comprometido de la mácula, si nos pasamos con el láser, podemos comprometerlo aún más. Cuando la retina se queda sin riego sanguíneo, deja de funcionar, y eso ya no se puede resolver.
Fotocoagulación para el edema difuso
A veces no encontramos lesiones individuales que podamos responsabilizar del edema macular. Toda la microcirculación de la mácula está mal, y se escapa fluido de forma difusa. No podemos cerrar indiscriminadamente vasos sanguíneos. En este caso hay varias estrategias, que consisten en dar láser en las zonas circundantes al centro, no ya individualmente a las lesiones, sino por áreas. Tienen varios nombres en función de la técnica utilizada: rejilla, rejilla modificada, hemirrejilla, etc.
El pronóstico no es bueno,: las posibilidades de que solucionemos el edema sin poder identificar bien las lesiones, es bajo.
Los impactos de láser en la mácula son más suaves que los que hacemos en la retina periférica, por lo que muchas veces no se ven con el característico color amarillo. Pero cuando hacemos una angiografía del ojo, los impactos de láser en la mácula se ven muy bien:
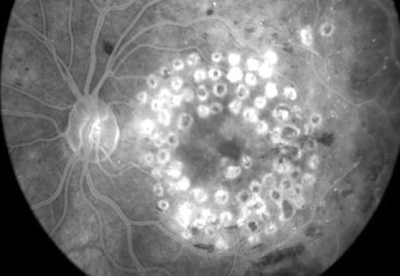
Causas de fracaso del tratamiento láser
Una causa la acabamos de decir: si el edema macular no es focal (uno o unos pocos puntos de fuga) sino difuso, es difícil neutralizarlo.
Otras veces se trata de un problema crónico: el líquido al principio se reparte entre las células, infiltrándose en el espacio extracelular. Pero con el paso del tiempo el líquido se reúne formando espacios quísticos, por lo que el tejido se desestructura más. Los grandes acúmulos de lípidos (moléculas grasas, lo que explicábamos antes de los exudados duros), cuando se sitúan en el centro de la mácula, también constituyen un problema. Estos cambios que se producen en el edema macular crónico disminuyen las posibilidades de éxito. Digamos que el líquido y otras moléculas que se han ido escapando de los vasos sanguíneo van modificando la estructura de la retina, que se va deformando y adaptando para dejarles espacio.
En un primer momento, la mácula es compacta y elástica, de forma que si «cerramos el grifo» al ocluir con láser los puntos de fuga, la propia retina vuelve a recuperar su estructura. Con el paso del tiempo, el tejido se «da de sí», se va modificando de forma que aunque neutralicemos los «escapes», el líquido y las moléculas grasas ya no se van.
¿Exito?
Por otra parte, cuando hablamos de éxito del tratamiento, debemos tener los pies en la tierra. Si las cosas van bien, conseguimos disminuir el espesor de la retina, y en la siguiente revisión (varias semanas o meses después del láser) constatamos un adelgazamiento (la mejor forma de objetivarlo es por OCT). El láser, en ese caso, ha funcionado. Eso no quiere decir que recuperemos visión, ojo. Algunas veces sí, hay mejoría visual y el propio paciente nos lo dice, pero muchas otras veces no, el daño que ha realizado el edema, no se revierte. Pero al disminuir el edema (idealmente, si conseguimos que la mácula recupere un espesor normal o casi normal) estamos previniendo que el paciente siga perdiendo visión.
Otras veces el láser no revierte el edema, pero por lo menos lo controla: no va a más. Algo es algo.
Neovascularización
Decíamos en el capítulo anterior que la complicación más temible de la retinopatía diabética es la aparición de neovasos, y las consecuencias que éstos producen. Aunque se suelen ver a simple vista, la angiografía fluoresceínica (AFG) de la que hablábamos antes los identifican muy bien. Como son vasos con la pared defectuosa, dejan escapar mucho contraste. Ya no es el lento fluir en los «puntos de fuga» del edema macular, sino que se acumula y escapa contraste muy rápidamente en los neovasos, identificándose claramente en las imágenes angiográficas como zonas muy blancas, muy brillantes.. Esto nos puede servir para seguir la evolución: tras el tratamiento, los neovasos en regresión captan menos contraste.

Decíamos que los neovasos se producen como respuesta a la isquemia de la retina, a que se queda sin el suficiente aporte de oxígeno. ¿Qué podemos hacer?. No, «quemar» los neovasos con láser no es una opción: sus pareces son muy delicadas y sangrarían en seguida. Además, no vamos a cerrarlos con calor (no tienen nada que ver con los pequeños microaneurismas que sí podemos cerrar con láser). No, debemos tratar el problema más en el origen.
La isquemia es un desequilibrio entre oferta y demanda. La retina tiene una demanda alta de oxígeno, hay muchas células (neuronas, fotorreceptores) que gastan mucho. La oferta de oxígeno cuando los vasos sanguíneos están sanos cubren bien la demanda. Pero en la diabetes, estos vasos no están sanos. No es que no funcionen nada (la retina no se queda totalmente sin oxígeno): el deterioro lento y progresivo va disminuyendo la oferta, hasta que llega un momento que no cubre la demanda. A partir de entonces, hay áreas de la retina que están isquémicas, y que producen señales químicas. Cuando hay una concentración suficiente de estas señales, se originan los neovasos. Hay que tener en cuenta que se trata de una respuesta global, entendiendo la retina como su conjunto. Si hay un área de isquemia muy pequeña, no habrá suficiente concentración de señales químicas para producir neovasos. Y cuando, desde las diferentes áreas isquémicas, la concentración alcanza cierto valor, los neovasos aparecen, pero no en las áreas de isquemia, sino donde el neovaso lo tiene más fácil para surgir (principalmente en el nervio óptico y a lo largo de los grandes vasos retinianos). Por tanto no es un problema local en la retina, es un problema general.
¿Qué podemos hacer?. Para restaurar este equilibrio entre oferta y demanda, lo ideal sería volver a restaurar la oferta haciendo que los vasos sanguíneos vuelvan a funcionar bien. Pero no podemos revertir el deterioro sufrido, así que actuamos sobre el ótro término de la ecuación: disminuimos la demanda.
¿Cómo hacerlo?. Si con el láser vamos produciendo quemaduras en la retina, esas zonas, aunque funcionen un poco peor, necesitarán menos oxígeno. Decíamos antes que la mácula es la zona de máxima visión, en especial en su centro (la fóvea), que es intocable con el láser. Pero la mayor parte de la retina no es mácula. La mayor parte de la superficie retiniana, y por tanto el mayor gasto de oxígeno, está fuera de la mácula. Y en estas zonas periféricas, una quemadura de láser produce poco efecto en la visión. Se vuelve una retina menos sensible al estímulo luminoso, pero sigue transmitiendo información. Y de esta retina periférica apenas necesitamos más: la visión fina, la más útil, se produce en la mácula, que no la vamos a tocar.
Así que eso es lo que vamos a hacer: cubrir toda la retina, excepto la mácula, de impactos de láser. Se denomina panfotocoagulación retiniana, fotocoagulación panrretiniana o panretinofotocoagulación (el prefijo «pan-» significa «todo», porque fotocoagulamos toda la retina menos la mácula). Por lo tanto, disminuimos la demanda de oxígeno. En el momento en que ésta queda por debajo de la oferta, se dejan de producir señales químicas que estimulen los neovasos. Y estos neovasos, sin las señales químicas, regresan: se vacían de sangre, empequeñecen y si hay suerte, desaparecen. Todo depende de lo a tiempo que tratemos la enfermedad: si los neovasos llevan poco tiempo, todavía hay esperanzas para ese ojo. A veces hay grandes crecimientos de neovasos y tejido fibroso en el interior del ojo y sobre la retina, y ese tejido ya no regresa.

En esta foto vemos una retina panfotocoagulada. Vemos los impactos de láser como «manchas amarillentas» muy regulares y del mismo tamaño, que ocupan toda la retina menos la mácula.
Otros tratamientos
El tratamiento principal es el láser, pero hay más, que utilizaremos algunas veces cuando el láser fracase o no podamos realizarlo.
En el edema macular, existen fármacos que impiden el escape de líquido desde los vasos sanguíneos. Estos medicamentos que disminuyen la permeabilidad vascular tienen tres grandes inconvenientes:
– Se deben utilizar localmente, en la cavidad vítrea. Eso supone inyectar el medicamento dentro del ojo. Con los posibles efectos secundarios que implica esa inyección.
– Algunos de estos fármacos tienen adicionalmente efectos secundarios en el ojo, que pueden ser importantes.
– Quizás lo más importante: su efecto, en general, es pasajero. Durante el tiempo que dura el efecto el edema disminuye, incluso puede haber una mejoría visual evidente. Pero no hemos solucionado el problema: la mala circulación de la mácula seguirá produciendo edema en cuanto desaparezca el efecto del medicamento. El láser es, por lo menos, algo más definitivo: nos da mayor margen y a muchas veces estabilizamos indefinidamente esa mácula.
Por tanto surge el problema: si es habitual que el tratamiento no resuelve el problema, ¿podemos tener al paciente cada dos por tres recibiendo un tratamiento que no es inocuo?.
Para los neovasos tenemos más o menos lo mismo: un medicamento inyectado dentro del ojo que inhibe las señales químicas que estimulan los neovasos. El efecto es más inmediato (y a veces, espectacular) que el láser. Podemos conseguir que los neovasos regresen. Nuevamente, no hay milagros: si hay una proliferación grande, el tejido fibroso no desaparece. Pero tenemos el mismo problema: el efecto es transitorio. Aquí, el tratamiento láser bien dado es muy eficaz: no es como en el edema macular que es frecuente que no funcione. Además es mucho más seguro, no metemos una aguja en el ojo. Por lo tanto, si cuando hay neovasos lo «definitivo» es el láser, ¿para qué pinchar antes?.
Así que habitualmente hacemos directamente panfotocoagulación, sólo planteamos comenzar con la inyección intraocular cuando las cosas están muy mal y tenemos que ganar tiempo, o cuando por alguna causa no podemos dar láser en este momento (por ejemplo, el ojo ha sangrado y la propia sangre impide dar láser). Pero es una medida transitoria, la idea es que nos dé tiempo para poder dar láser.
Cuando los neovasos han complicado el cuadro, tenemos que operar. Mediante una cirugía similar a la explicada en el artículo del desprendimiento de retina (una vitrectomía), eliminamos el gel vítreo, quitamos la sangre que hubiera delante y nos estorbaba para dar láser, reparamos el desprendimiento de retina si lo hubiera, intentamos quitar alguna membrana neovascular (si podemos), e incluso podemos dar láser dentro de la operación.
También se ha planteado hacer este tipo de operación en el edema macular, aunque la justificación no es tan clara (lo es en determinadas circunstancias, pero tampoco quiero alargar mucho este artículo).
Los tratamientos más utilizados de la inyección intraocular pertenecen principalmente a dos tipos de familias:
– Corticoides: son antiinflamatorios muy utilizados en medicina. En la retinopatía diabética, se han principalmente para el edema macular. Pueden producir efectos secundarios (aumento de presión intraocular, cataratas).
– Antiangiogénicos: Tenemos menos años de experiencia en su uso intraocular comparado con los corticoides. Tienen bastantes menos efectos secundarios que los corticoides. Como su nombre indica, inhiben la angiogénesis, la aparición de vasos sanguíneos. Por tanto van bien contra los neovasos. Estos mismos fármacos se utilizan en otra enfermedad ocular que también cursa con crecimiento vascular: la degeneración macular asociada a la edad, en su forma húmeda. Ya mencionamos este tratamiento en el artículo enlazado. Curiosamente, estos factores pro-angiogénicos (que estimulan los neovasos y son inhibidos con el fármaco) también juegan un papel en el edema macular, por lo que los antiangiogénicos también son eficaces para dicho edema. El problema es que le pasa lo mismo que con los corticoides: el efecto es pasajero. Además, la experiencia utilizando antiangiogénicos en el edema macular es menor que usando corticoides. Sin embargo, debido a los importantes efectos secundarios de estos últimos, cada vez hay más estudios científicos que evalúan la eficacia de los antiangiogénicos en el edema macular.
Como véis, la utilización de medicamentos intraoculares es lo más nuevo, pero no es la panacea y aunque son eficaces está por ver cuánto de eficaces son, y hasta cuándo. El problema a la hora de utilizarlos es que no es el tratamiento aprobado por los diferentes ministerios y agencias sanitarias. Es decir: un oftalmólogo puede y debe tratar con láser la retinopatía diabética. Es lo que está demostrado y aprobado. El uso de fármacos intraoculares es más complejo: no están aprobados oficialmente para uso intraocular (ojo, hablo de la retinopatía diabética), incluso aunque ya dispongamos de evidencia científica sólida de su eficacia y su perfil de seguridad. Por lo tanto, si de la utilización de ese fármaco derivan complicaciones (no olvidemos que es una inyección en el ojo), el médico no está muy cubierto legalmente si los aplica como «tratamiento convencional». En la mayoría de las ocasiones debe utilizarse el llamado «uso compasivo», que consiste en emplear tratamientos no aprobados todavía por el ministario, cuando no hay más alternativas. Pero eso supone enviar un informe personalizado, que éste nos lo apruebe….. una serie de trabas.
Teniendo en cuenta que, sobre todo para el edema macular, puede que sólo ofrezcamos una mejoría transitoria, pues no está tan claro si tratar o no tratar, y a quién tratar.






6 noviembre, 2008
Buenas,
Aunque vaya un poco a contratiempo del articulo, queria comentar una curiosidad sobre los antiangiogenicos. He leido que su uso en oftalmologia se descubrio por casualidad, bueno, supongo que tambien despues de varios estudios, y visto lo visto aun queda mucho por andar a pesar de las expectativas sobre todo lo novedoso. Volviendo al tema, el supuesto descubrimiento casual se produjo en pacientes con cancer, y ellos empezaron a notar que veian mejor. Entonces no se les pinchaba en el vitreo; no se como se los aplicarian, pero se beneficiaban indirectamente sus ojos(temporalmente, imagino). Empezaron mas o menos asi las cosas o no?
Un saludo.
4 noviembre, 2016
Buenos días, me ha encantado el blog y su contenido. Enhorabuena por el contenido que aunque es del 2009, según creo es bastante bueno.
Un apunte al hilo de lo que comenta Adela, el Avastín SÍ que comenzó como antitumoral y de hecho sigue usando en la terapia contra el cáncer de colon.
No sé a quien se le ocurrió usarlo por vía intravítrea, es decir no sé como se le ocurrió usar en el ojo un tratamiento que se usaba para el … (otro ojo ;- ) pero claramente fue como medicación «off-label», y gracias a ese médico, tenemos el que ha sido el mejor tratamiento hasta ahora. El avastín se está dejando de usar no porque no sea útil, sino por intereses farmacéuticos, pero eso es ya otro tema…
Un saludo y espero que este blog siga animándose
25 noviembre, 2008
Hola Ocularis,
Se te ha pasado responder al comentario anterior sobre retinoptatia diabetica?
Un saludo.
25 noviembre, 2008
Pues sí, se me pasó contestarlo. Suelo aprobar los comentarios y contestarlos inmediatamente. Recuerdo que leí tu comentario y pensé la respuesta, de hecho creía que había contestado.
No te puedo contestar con total seguridad, pero tengo importantes razones para dudar de esa afirmación:
– Desde hace tiempo la investigación iba detrás de una sustancia que inhibiera la angiogénesis. Se había probado con corticoides intravítreos, que tiene un buen efecto sobre la inflamación y el edema. Ya se utilizaban en medicina otras sustancias más específicas contra el crecimiento vascular, con lo que el campo de investigación estaba claro.
– Para que tenga efecto, estas sustancias se deben inyectar dentro del vítreo. Por vía sistémica no funcionan (si lo harían, aunque fuera como ayuda y en pequeñas dosis, se realizaría así porque las inyecciones en el ojo suponen un riesgo importante). Por lo tanto, no se sostiene mucho que utilizado por vía sistémica para otra cosa se produzca mejoría. Teniendo en cuenta además que lo que hacen los antiangiogénicos principalmente es parar el cuadro. La mejoría visual, caso de que se produzca, suele ser discreta, y si no hay un oftalmólogo monitorizando la lesión, es difícil que uno se de cuenta.
26 noviembre, 2008
Desde luego no se puede dar mucho credito a todo lo que aparece escrito por internet aunque tenga pinta de cientifico y tal. Las cosas siempre suelen ser mas complejas.
26 noviembre, 2008
Pues sí, es saludable tener pensamiento crítico.
Gracias por leerme.
27 noviembre, 2008
Nada, un placer.
Larga vida al blog.
18 agosto, 2009
Hola ocularis
Mi pregunta es de una persona poco entendida en oftalmologia
Quisiera saber cuando esta aconsejado iniciar el tramiento especializado ( ya sea laser o otro) en la retinopatia diabetica. Creo que es ya en fases de retinopatia proliferatica o cuando hay edema macular
gracias
25 agosto, 2009
En este artículo hablo de los diferentes tratamientos láser para la retinopatía diabética. En principio debería estar contestada tu pregunta. Concretar o personalizar más significa tomar una decisión médica. En otras palabras: cuándo está aconsejado iniciar el tratamiento depende de tu oftalmólogo.
Un saludo.
11 septiembre, 2011
[…] resumen, poca información. En el artículo de este blog que dedico al tratamiento de la retinopatía diabética sí me extiendo más a explicar cómo funciona esta fotocoagulación panrretiniana que es el tema […]
28 diciembre, 2014
[…] procedimiento es el tratamiento indicado para pacientes diagnosticados con Retinopatía Diabética, que produce sangrados en la […]