En el artículo previo nos hemos puesto al día del tratamiento de base de la degeneración macular asociada a la edad (DMAE). Hemos visto que los productos que venden para prevenir y frenar la evolución de la enfermedad, los suplementos nutricionales con vitaminas y antioxidantes, no funcionan y no se deben utilizar. La evidencia científica está ahí, y ya las guías clínicas están comenzando a tener un papel activo desaconsejando el uso de estos productos. Es decir, que está claro lo que es correcto, y que se puede hacer lo correcto, aunque debido a la inercia y a diversos conflictos de intereses, costará llevarlo a la práctica.
El tema de hoy es algo más difícil, porque no está tan claro qué es lo correcto. O, mejor dicho, hay escollos serios para llevar a cabo lo que es correcto.
La membrana neovascular
La degeneración macular asociada a la edad (DMAE) es una degeneración progresiva de la mácula que es la retina central. Esta enfermedad puede llegar a producir pérdidas visuales importantes. En el artículo anterior he puesto varios enlaces donde explico en más profundidad las características de la DMAE.
Este deterioro lo podemos clasificar como relativamente lento. Puede ocurrir, sin embargo, que sobre una DMAE previa, “de base”, aparezca una complicación. Esta retina cuyas células van degenerando y muriendo está predispuesta a que aparezca un tejido por debajo, cuyo origen está en la parte del ojo sobre la que esta retina se apoya (la coroides). Este tejido nuevo prolifera a modo de “cicatriz”, con vasos sanguíneos y tejido fibroso. Adquiere la forma de membrana que crece en el plano entre la retina y la coroides. Puede ser transparente al inicio, por lo que no siempre es fácil de detectar. Tiende dejar fluido a su alrededor, y luego a sangrar. Deteriora rápidamente la visión y produce un daño acelerado de la retina. Es decir, cuando sobre una DMAE crece una membrana neovascular, se pierde vista de forma acelerada.
En la clasificación antigua de la enfermedad, a la DMAE como tal se denominaba “forma seca o atrófica” y cuando tenemos una membrana neovascular se denominaba “forma húmeda o exudativa”. Ahora la denominación es otra, conviene saber que cuando leamos en algún sitio “DMAE húmeda” o “DMAE exudativa” (en inglés “wet AMD” o “exudative” AMD”) nos estamos refiriendo a lo mismo: la membrana neovascular.
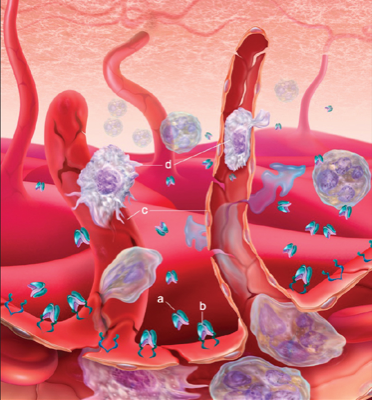
En cualquier caso, la membrana neovascular (también denominada neovascularización coroidea, membrana subrretiniana o membrana submacular) es una complicación terrible que amenaza seriamente la visión del que la padece.
Aunque estas membranas neovasculares también se pueden producir en otras enfermedades de la mácula (en miopes altos, inflamaciones oculares, etc.) y el tratamiento propuesto es el mismo (las inyecciones de antiangiogénicos, como explico más abajo), a lo largo de este artículo me iré refiriendo solamente a la membrana secundaria a DMAE.
El tratamiento
¿Tiene tratamiento la membrana neovascular?. Sí. ¿Es eficaz?. En general, entre poco y moderadamente eficaz, y si se pilla a tiempo. Eso quiere decir que si el tratamiento llega tarde, no vamos a recuperar visión.
La evolución natural de la membrana es la siguiente: tiene un periodo de actividad en la que crece, acumula líquido bajo la retina, sangra, y produce un deterioro acelerado de la retina (la mácula, concretamente). Por sí sola, la membrana suele desactivarse a medio plazo, y para cuando llega ese momento la retina afectada (la mácula) por desgracia suele estar bastante deteriorada y se ha transformado en una cicatriz, con poca función visual. Dicha mácula no funciona y por tanto dejamos de ver por la zona central de nuestro campo visual, que es con el que reconocemos caras, leemos y hacemos todas las actividades de exigencia visual alta.

El objetivo del tratamiento es inactivar la membrana antes de que deteriore tanto la mácula y la visión. El tratamiento tiene, en algunos casos, esa capacidad de inactivar este tejido, y hasta cierto punto puede revertir algunos cambios precoces. Concretamente puede revertir el acúmulo de líquido bajo la retina, y puede que también ayude a eliminar el sangrado, o que no sangre más. El medicamento no revierte los efectos tardíos, la degeneración de las células de la retina.
Por lo tanto, si comenzamos a tratar en una etapa tardía, el paciente no va a recuperar la vista perdida. Incluso aunque obtengamos una mejoría “anatómica” (el líquido disminuye y la retina vuelve a una posición más normal), si la retina ha sufrido daños irreversibles, el paciente no verá mejor.
Cuando podemos poner el tratamiento en un estadío más precoz, la membrana se puede inactivar o no. Puede haber una recuperación visual inicial que el paciente lo puede notar. En casos poco frecuentes incluso puede ganar bastante visión. Esto ocurre porque al disminuir el fluido bajo la retina, podemos ver mejor. El problema es cuando el líquido disminuye pero la membrana realmente no se inactiva. En estos casos, justo tras el tratamiento recuperamos visión, pero al poco tiempo perdemos de nuevo, porque la membrana sigue activa y suelta líquido de nuevo. Tras ese poco tiempo habría que volver a poner el tratamiento. Hay casos de estos que ponemos muchos tratamientos y parece que conservamos la visión, pero la evolución de la membrana realmente no se ha frenado, y a largo plazo la pérdida de visión se instaura.
Las grandes preguntas clínicas
En resumen, los resultados del tratamiento son muy variables. Una cuestión difícil de resolver es cuándo debemos tomar la decisión de no iniciar un tratamiento porque simplemente ya es tarde. Está claro que es una decisión dura de tomar, pero por mucho que cueste debemos asumirla con objetividad. Evitarla simplemente aplicando el tratamiento a todos los casos, aunque se hace con mucha frecuencia, no es correcto desde el punto de vista objetivo, humanitario, ni siquiera deontológico. Me explico: sabemos a ciencia cierta que en los casos tardíos el tratamiento simplemente no va a funcionar, y sometemos al paciente (como explicamos más abajo) a un riesgo porque el tratamiento es intervencionista, en algunos aspectos similar a una cirugía. Además del trastorno que le producimos al paciente y a los familiares, y el enorme coste que supone para el paciente o el sistema el aplicar un tratamiento ineficaz.
Lo mismo ocurre a la hora de suspender el tratamiento. Aunque lo hayamos indicado de forma adecuada, en una situación en la que a priori tenemos unas probabilidades razonables de que funcione, hay una alta tasa de no respondedores. Eso quiere decir que en una proporción importante de pacientes no va funcionar. Debemos identificar a estos no respondedores, y en ese caso suspender el tratamiento. Por los mismos motivos que antes: si ya podemos establecer objetivamente y con seguridad que el tratamiento no funciona, lo ético y razonable es dejar de tratar, por los motivos de riesgos, pérdida de calidad de vida del paciente y acompañante, y costes.
Simplificando, las grandes preguntas que debemos contestar son:
- ¿Cuándo no comenzar el tratamiento?
- ¿Cuándo suspenderlo?
Son decisiones difíciles, tanto para el médico para decidirlo y llevarlo a cabo, como para el paciente para asumirlo. La decisión «fácil», en estos casos donde el tratamiento ya no funciona, es seguir poniéndolo, aferrándonos a vanas esperanzas.
El funcionamiento
Ya hemos visto los problemas a los que se enfrenta este tratamiento. Veamos ahora cómo funcionan los fármacos utilizados.
Las membranas están formadas por tejido vascular neoformado; es decir, vasos sanguíneos que se crean de novo, que antes no existían. Esta proliferación está mediada por unas señales químicas, siendo una de ellas (quizás la más importante), el llamado VEGF, factor de crecimiento vascular endotelial.
Disponemos de un tratamiento que bloquea la función de esta señal química, del VEGF. Se llamarían anti-VEGF, o simplemente antiangiogénicos. Es medicación que bloquea la angiogénesis, la generación de nuevas arterias.
¿Todos estos nombres raros son muy complicados? ¿Lo de señales químicas, vasos de novo, angiogénesis y demás te suena a chino?. No pasa nada, entender todo esto no es esencial. Lo apunto para aquellos más metidos en el tema, para que tengan más información. Simplemente hay que entender que este fármaco a veces es capaz de “parar” la progresión de la membrana.
Para conseguir concentraciones adecuadas de este medicamento en la membrana neovascular no sirve inyectarlo en sangre. Tampoco se puede tomar por la boca. Debemos inyectarlo en el interior del ojo. Lo cual impone el primer escollo de esta medicación: una inyección en el ojo es un procedimiento intervencionista, con unos riesgos.
Con una sola inyección no vamos a inactivar una membrana neovascular. Incluso en los casos en los que este tratamiento funciona bien, de forma inicial vamos a ir inyectando una vez al mes entre 3 y 5 veces. Y luego habrá que revisar cada 1-2 meses, y si encontramos signos de actividad (por ejemplo, que aumente el líquido bajo la retina), repetir la inyección. Inactivar la enfermedad puede suponer fácilmente 8 inyecciones al año, o más.
Hay otras pautas más intervencionistas en las cuales no se repite la inyección solo cuando parece que empeora, sino que siempre que revisamos al paciente le inyectamos el fármaco, esté bien o mal. Si está bien, posponemos un poco la siguiente visita (donde le inyectaremos igualmente). Hay diferentes sistemas, parece que no está claro cuáles son mejores que otros. En cualquier caso, incluso las pautas más conservadoras implican numerosos tratamientos.
Tanta inyección implica un riesgo para el paciente, como decíamos antes. El ojo se puede infectar, puede sangrar por dentro, se puede desprender la retina. Por cada inyección el riesgo es bajo, pero si tenemos que pinchar muchas veces, vamos a acumular un riesgo que en global ya no es tan bajo. Un aspecto que no podemos ignorar. También deberíamos tener en cuenta el efecto crónico acumulativo de la medicación, y algunos artículos así lo apuntan. El uso de inyecciones repetidas parece tener efectos perjudiciales en la retina.
A eso se le añade la cantidad de veces que el paciente tiene que acudir a la clínica o al hospital, tanto para las inyecciones como las revisiones. Muchas citas cada año en personas mayores que igual no están en las condiciones ideales. Supone un trastorno para ellos y para la familia o cuidadores, además de la ocupación de muchos recursos del sistema sanitario.
Esto último, lo de ocupar recursos del sistema, a veces no se entiende bien desde el punto de vista del paciente. Nos gusta pensar que el sistema sanitario es suficientemente flexible para ofrecernos siempre las opciones diagnósticas y terapéuticas cuando las necesitamos. Eso no es así. Hay que tener en cuenta que los recursos son limitados, y muy habitualmente ya están al límite de su capacidad. En España la mayoría de tratamientos antiangiogénicos se llevan a cabo en la sanidad pública. Para cada área sanitaria, el número de oftalmólogos es el que es, normalmente por debajo de la demanda real. Es habitual que los huecos disponibles para consulta y quirófano estén sobresaturados. Para el diagnóstico y el seguimiento de las membranas neovasculares se necesitan pruebas diagnósticas (tomografía de coherencia óptica, angiografía) que se llevan a cabo con aparatos caros de los que se disponen de pocas unidades, y solo en hospitales de tamaño medio y grande. Los recursos (oftalmólogos, resto de personal, aparatos, quirófanos) que invertimos en el manejo de esta enfermedad, no lo dedicamos a otras. Y si el tratamiento no funciona, aparte del perjuicio para ese paciente concreto que le estamos «pinchando el ojo», además estamos dejando de emplear esos recursos para pacientes con enfermedades que sí pueden beneficiarse de diagnosticarse o tratarse.
Vamos a poner un ejemplo: una persona de 85 años con dificultades de movilidad y una membrana neovascular en un ojo, que en el momento del diagnóstico ya tiene la visión de ese ojo deteriorada. Actualmente «se maneja» con el otro ojo. Este ejemplo sería un caso típico, muy habitual. La primera decisión compleja es si iniciar el tratamiento. Puede que ya no lo hayamos cogido a tiempo. Supone un trastorno importante acudir muchas veces al hospital, pincharle el ojo 6, 8 ó 10 veces en un año, para que funcione el medicamento, o no. Si funciona algo, probablemente el paciente se siga manejando con el otro ojo, y esa “mejoría de visión” que nosotros certificamos en la consulta, midiendo la agudeza visual, no repercuta en mejor calidad de vida del paciente. Lo que sí que hemos hecho ha sido deteriorar su calidad de vida haciéndole venir al hospital, con las inyecciones, exigiendo un esfuerzo importante a los cuidadores. Y eso si tenemos suerte y no sufre alguna complicación por tantas inyecciones.
Y por otra parte, el problema indirecto. ¿Cuántas horas de oftalmólogos, enfermería y el resto de personal invertimos en ello?. Tiempo de uso de aparatos diagnósticos, de salas estériles y quirófanos, etc. Luego para otras enfermedades los pacientes tienen que esperar. Una espera que puede repercutir en el pronóstico de su problema.
Los riesgos, los importantes inconvenientes de un tratamiento repetido, las consecuencias indirectas, son problemas de primer orden difíciles de resolver. Las decisiónes clínicas que explicábamos antes de cuándo tratar, cuándo no tratar, cuándo cesar el tratamiento, es compleja, y sometida a mucha presión. Pero ahora vamos a enfocarnos en el problema del coste.
Antiangiogénicos oficiales
Existen, tanto en España como en el resto de Europa, Estados Unidos y otros muchos países, dos medicamentos aprobados por las autoridades sanitarias para el tratamiento intraocular de la membrana neovascular causada por la degeneración macular asociada a la edad. Uno es el ranibizumab (Lucentis ®, de Novartis), y el otro es el aflibercept (Eylea ®, de Bayer).

Ambos medicamentos han demostrado su eficacia a corto plazo en un porcentaje de pacientes. Como decíamos más arriba, no funcionan en etapas tardías, y cogido a tiempo hay pacientes no respondedores (que no les hace efecto). En los pacientes respondedores, no son pocos los que acabarán con mala visión, y el tratamiento solo les estaba dando unos meses o a lo sumo 1-2 años de mejor visión antes de que acaben mal. Pero sí que han demostrado su eficacia a nivel «científico» digamos (lo podemos medir) y a corto-medio plazo.

En fin, lo que explicábamos en los párrafos de arriba, pero a esto vamos a añadir el tema del coste. La cantidad de medicación que utilizamos en cada inyección es muy pequeña, del orden de 0,05 mililitros. Eso son como 3-4 gotitas. Cada inyección con 0,05 ml cuesta entre 700-800 euros. Para una pauta de unas 8 inyecciones anuales, que sería una estimación bastante conservadora, serían en torno a 6.000 €. Por paciente y año. Mucho, ¿verdad?.
¿Cómo puede ser que una dosis de medicación tan baja pueda ser tan absurdamente cara?. Porque ese precio no refleja los costes de fabricación, evidentemente. La postura de las empresas que lo venden es que hay que amortizar los gastos de investigación. Por otra parte, se trata de una enfermedad muy frecuente, con una gran demanda, y la realidad es que nos enfrentamos a un oligopolio de facto. Solo hay dos productos y no entran en lucha de precios. Así que otra lectura de la situación actual sería la siguiente: simplemente imponen los precios porque pueden, y porque la gente va a pagarlo igualmente.
El caso es que ése es el precio que hay.
El otro angiogénico
Los medicamentos anti-VEGF no son nuevos, ni se usan por primera vez ni principalmente para la degeneración macular. Uno de los campos donde más se utilizan es en el cáncer. Los tumores producen este factor de crecimiento vascular endotelial (VEGF), lo que hace que se formen nuevos vasos sanguíneos que alimentan las células tumorales. El uso de anti-VEGF cierra esos vasos sanguíneos anómalos e impide que se produzcan nuevos. Eso puede parar el crecimiento e incluso reducir el tamaño del tumor.
Nuevamente, hacemos una parada. ¿todo esto es demasiado técnico?. No te preocupes, no es importante. Simplemente hay que entender que usamos los mismos medicamentos para otras enfermedades, por lo que ya hay experiencia en la fabricación y el uso de estos compuestos, e incluso han desarrolladas otras moléculas similares.
Estos antiangiogénicos que se usan para el cáncer no son de por sí baratos, pero se necesitan volúmenes altos, porque se usan por vía intravenosa. Hablamos de precios por litro, no se venden dosis de millonésimas de litro, como en el caso de los antiangiogénicos para el ojo.
Uno de estos antitumorales es el llamado bevacizumab (Avastin ®, de Roche). Tiene de especial que la molécula es muy similar a los que hemos comentado antes, a los “oficiales” ranibizumab y aflibercept.

El bevacizumab comenzó a utilizarse para tratar las membranas neovasculares en inyección dentro del ojo, y funcionaba. Como hemos explicado más arriba, no era eficaz en todos los casos; solo en algunos donde se cogía a tiempo, y no de forma indefinida. Pero funcionaba. Se pincharon miles y miles de ojos, y se evaluó su eficacia y seguridad. Luego se comparó con la otra alternativa, el ranibizumab (el Lucentis ® que apareció primeramente). Los resultados tanto en eficacia como en seguridad eran similares entre ambos medicamentos.
El aflibercept (Eylea ®) se comercializó bastante tiempo después. Como vamos a hablar de lo que se hizo al principio, nos olvidaremos del aflibercept por ahora.
En aquellos años, cuando no se había aprobado oficialmente ninguno de estos medicamentos para tratar la membrana neovascular asociada a la DMAE, se podían utilizar libremente cualquiera de estos medicamentos. ¿Cómo? ¿Si no hay un medicamentos aprobado, el médico tiene más libertar para ofrecer el tratamiento?. Pues con matices, pero así es.
La trampa legal
El Ministerio de Sanidad de cada país, o el organismo gubernamental análogo, a través de la agencia del medicamento, es el encargado de establecer qué medicamentos están oficialmente aprobados para cada una de las enfermedades. El médico en principio ofrecerá a su paciente el tratamiento que crea indicado, pero dentro de los que estén aprobados oficialmente. Este sistema de control y regulación es bueno, porque se supone que la aprobación oficial se obtiene mediante evidencias científicas. Desde el punto de vista del paciente es una garantía adicional. Además de la actuación del médico, del se se espera y exige una actuación de acuerdo a la evidencia científica disponible, el organismo sanitario competente garantiza que el tratamiento que uno vaya a recibir tiene un respaldo científico detrás. Si un médico indica un medicamento no basado en pruebas científicas, dicho medicamento no tendrá aprobada la indicación oficial por el ministerio, por lo que dicho médico puede incurrir en un delito. Eso es una medida disuasoria para aquellos médicos que tengan la tentación de hacer mal las cosas. Y por lo tanto es una forma de proteger al paciente.
Para que un medicamento obtenga esta aprobación por parte del ministerio de Sanidad, la empresa que fabrica el producto tiene que solicitarla. Debe reunir los estudios científicos que respaldan su eficacia y seguridad, y además llevar a cabo un largo proceso burocrática. Entre que hay evidencia científica para utilizar un medicamento y llega la aprobación oficial pasan años. En ese tiempo, los médicos están al tanto de que hay un medicamento que es útil para una enfermedad, pero no tienen aprobación oficial. Puede darse el caso, y de hecho ocurre de forma muy frecuente, que para una enfermedad concreta no han ningún medicamente oficialmente aprobado. Con lo cual no hay nada que ofrecer de forma oficial y legal. Sin embargo, algunos principios activos sí pueden tener evidencias de su seguridad y eficacia, aunque todavía no tengan la aprobación oficial. Para esta situación concreta, se puede realizar una indicación terapéutica especial llamada “de uso compasivo”, o en inglés “off-label”. Se supone que es una medida transitoria, hasta que llegue la aprobación oficial de los medicamentos que lo han solicitado. Al paciente se le informa de todo ello, y es el que toma la decisión final.
Así es como funciona de forma general la indicación normal de medicamentos y el uso compasivo. Esto es importante para lo que nos ocupa hoy, y para aquel momento. Por aquel entonces había membranas neovasculares y ningún antiangiogénico oficialmente aprobado. Tanto el ranibizumab como el bevacizumab contaban con respaldo suficiente como para comenzar a utilizarlos como uso compasivo. Y así fue. Se trataron miles de ojos con uno y con otro. Se hicieron comparaciones de eficacia y seguridad. Los resultados eran similares. Solo que el bevacizumab, un medicamento que se utilizaba para otra cosa y que se vende en litros, resulta mucho más barato. Preparar en un hospital una inyección de 0,05 ml de bevacizumab cuesta menos de 10 euros. Frente a los cerca de 800 euros del ranibizumab.
Evidentemente, en muchas partes se prefirió el uso del bevacizumab. Era un medicamento no muy eficaz en muchos casos, pero de eficacia y seguridad similar al otro, pero mucho más barato.
Finalmente, llegó la aprobación del ministerio. Y llegó para la empresa que lo había solicitado. Novartis había creado el ranibizumab para su uso intraocular en esta enfermedad (luego también para otras), y obtuvo la autorización que pidió. Roche, la farmacéutica del bevacizumab, no estaba comercializando el medicamento para el uso oftalmológico. No preparaba pequeñas dosis para tratar las membranas en la retina. Vendía envases grandes para otro uso, y en los hospitales y clínicas preparaban las dosis que se utilizaban en el ojo. Como no solicitó aprobación ninguna para que se usara su medicamento en el ojo, no lo obtuvo.
Y así se llegó a la situación en la que había un producto que estaba aprobado, el ranibizumab. En estas circunstancias, ya no puedes optar por ofrecer un uso compasivo u “off-label”. Decíamos que esa era una medida transitoria en los casos en los que no hay ningún medicamento disponible autorizado. Cuando hay por lo menos uno, ya no puedes ofrecer una alternativa que no cuenta con la autorización oficial.
Y es una situación muy anómala, porque un tiempo antes sí has podido ofrecer una alternativa sostenible, con un precio razonable y asumible. Se ha acumulado gran experiencia que avala la eficacia (no grande, pero similar a la opción oficial) y la seguridad del bevacizumab. Sabemos que podemos utilizar el bevacizumab, que tenemos garantías científicas para ofrecerlo en igualdad de condiciones, y sin embargo no podemos hacerlo.
En el fondo, es una trampa legal, un tecnicismo. El sistema no contempla que un medicamento pueda funcionar, sea la alternativa de elección para una enfermedad y que la empresa no solicite la autorización de uso. Y no pueden ser ni los propios médicos, ni las autoridades científicas, ni ningún organismo el que impulse la autorización. Cuando se diseñó el sistema legal de uso y autorización de medicamentos no se contempló esta posibilidad. Así que el propio sistema, los usuarios y la propia sociedad estamos atrapados absurdamente en este callejón normativo.
Como resultado, los medicamentos autorizados son capaces de imponer unos precios desorbitados, que pueden lesionar gravemente el sistema sanitario público, sin tener miedo de la alternativa razonable.
Prácticas monopolísticas
La pregunta que surge inmediatamente es: ¿porqué los laboratorios Roche no solicitan la autorización para el uso de su bevacizumab?. Lo tienen muy fácil. Ya usan esa molécula para otra enfermedad, con éxito, con lo que los costes de investigación y producción los tienen amortizados *. Ya producen en serie la molécula. Simplemente en vez de dispensarlo en frascos con mucho volumen, en dosis mucho más pequeñas.
No tienen que llevar ellos los ensayos clínicos para demostrar su eficacia y seguridad: durante años los oftalmólogos clínicos les hemos hecho ese trabajo. En cuanto al estudio de mercado, lo tienen muy fácil: en la época en la que usábamos los antiangiogénicos por uso compasivo, el preferido era su medicamento. Ya tienen el mercado “ganado”, digamos. No tienen que promocionar ni dar a conocer su producto.
Aunque ya salen ganando dinero tal como lo venden su bevacizumab en litros, Roche pueden indicarlo con un coste de, pongamos, 100 euros la inyección. Casi todo ese dinero es beneficio para ellos. En comparación con su competencia, van a seguir siendo la opción más barata con mucho margen. Es un negocio redondo. ¿Por qué no lo hacen?.
En cuanto pensemos un poco mal, podemos adivinar lo que ha pasado. Novartis, la que está haciendo negocio con su ranibizumab, exprimiendo las arcas públicas de muchos países con un precio desorbitado, va a intentar por todos los medios que Roche no entre en el mercado con precios bajos. Simplemente llegan a un acuerdo económico y ya está. Yo te pago una buena cantidad de dinero para que no entres en este mercado. Bien para las dos empresas, fatal para nuestro sistema sanitario. ¿Esto puede sonar paranoia mía?. Pues no lo es. En Italia lo pudieron demostrar, y Novartis fue condenada por ello. No importa, los números con los que trabajan son muy grandes. Les sale a cuenta pagar la multa en Italia y pagar a Roche, los beneficios siguen compensando. Hay que tener en cuenta que son empresas multinacionales que operan en muchos países. Pueden asumir que en un país, Italia en este caso, tengan que dejar un «pequeño pico». Este «pequeño pico» son más de 90 millones de euros, y el tema todavía colea. Para el que quiera saber más, aquí tiene un comunicado del tribunal de justicia de la Unión Europea sobre el tema.
¿Hay solución?
¿Se puede salir de esta encerrona?. Se trata de una situación compleja, porque no es solo el propio reglamento, sino que hay tres de las empresas farmacéuticas más grandes (Novartis, Bayer, y curiosamente también Roche) las que se van a oponer, y son entidades multinacionales con grandes recursos económicos. Eso significa, entre otras cosas, equipos de abogados que harán todo lo posible para proteger los intereses de las empresas. Aunque signifique llevar a cabo acciones en contra de la salud pública.
Como decíamos, salir de este problema es difícil, pero no imposible. Es evidente que hay que utilizar la alternativa que por la evidencia científica disponible y por precio es asumible. Utilizar bevacizumab en vez de las otros dos principios activos. Diversos países europeos están tomando medidas para poder llevarlo a cabo. En el Reino Unido son los propios oftalmólogos los que se han manifestado en contra de de la situación y están moviendo las cosas a nivel oficial para poder usar el bevacizumab. La cosa va tan en serio que las farmacéuticas están yendo contra los oftalmólogos. En Francia ha ocurrido algo similar, aunque las autoridades movieron ficha antes. La agencia del medicamento francesa permitió el uso legal del bevacizumab ya en 2014. Por supuesto, las farmacéuticas (Novartis y Roche) se opusieron y llevaron al gobierno francés a los tribunales. En 2016 perdieron pero siguieron apelando, y en 2017 por fin el tribunal supremo francés cerró la vía judicial confirmando la decisión de la agencia del medicamento, protegiendo el sistema sanitario frances y a los propios franceses.

Es un tema complejo, porque la solución no puede ser simplemente acabar con las regulaciones sanitarias con respecto a la aprobación de medicamentos, y así dar vía libre a todo principio activo que se pretenda utilizar off-label. Se trata de consideraciones regulatorias nacionales, legales, judiciales y económicas, cuyos detalles se salen de lo que vamos a hablar en este blog. Pero está claro que algo hay que hacer, y otros países de nuestro entorno ya están buscando soluciones para rescatar al sistema sanitario y a nuestros propios pacientes de esta trampa legal.
Y mientras, ¿qué está haciendo España?. Lo explico en el próximo artículo.
—
* Realmente el asunto es más complicado, porque las dos moléculas (ranibizumab y bevacizumab) están producida por otra empresa llamada Genetech, que forma parte del grupo Roche. Genetech cede la explotación comercial del ranibizumab a Novartis a través de un contrato de licencia. Por lo tanto hay motivos para que estas empresas no entren en competencia entre ellas, aunque no quiero complicar este artículo con tanta trama empresarial.






25 enero, 2018
Se usaba la radioterapia a dosis bajas con aceptables resultados (y muchisimo más barato). Perooooo. Je
25 enero, 2018
Muy claro los artículos. Felicitaciones y gracias.
27 enero, 2018
Increible, gracias por difundir.
Saludos
27 agosto, 2022
[…] segundo lo dedico al problema de los antiangiogénicos, el tratamiento para la membrana […]
8 enero, 2023
[…] esa enfermedad se están desmandando cada vez más. Fueron tres artículos de actualización (uno, dos y […]